Publicado en Endocrinol Nutr. 2002; 49:299-307. - Vol.49 núm 09
La diabetes mellitus gestacional (DMG) sí asocia un aumento de la ONU de morbilidad Materna y fetal, y ESTO SE ha relacionado Con El control glucémico materno. Diversos Estudios Han descrito Que sin Tratamiento Intensivo El Disminuye Riesgo perinatal, y la monitorización domiciliaria de la glucemia capilar (AMGC) es Uno de los Principales Instrumentos párrafo ConTrolar El Tratamiento.Respecto de Los Objetivos del Tratamiento, Han disminuído en los Últimos Taller de Conferencias Sobre DMG acercándose al Rango de Normalidad, y actualmente sí aconseja conseguir glucemia capilar basal Una ¾ 95 mg / dl, 1 hora posprandial ¾ 140 mg / dl o 2 horas posprandial ¾ 120 mg / dl o incluso inferiores. Sin embargo, las Encuestas Sobre la Práctica Clínica habitual describen Amplias differences En El Seguimiento de las RECOMENDACIONES Tanto en la AMGC Como en los Objetivos del control glucémico. Por Otro Lado, TAMBIÉN SE ha Propuesto El Estudio de parametros fetales párrafo Valorar El control metabólico.
Texto completo
La diabetes mellitus gestacional (DMG) sí asocia un aumento de la ONU de la morbilidad Materna y fetal Tanto En El Período perinatal Como un largo Plazo. Se ha descrito la ONU alcalde de Riesgo de preeclampsia, hidramnios y Parto Por Cesárea, ademas de las Naciones Unidas alcalde Riesgo de macrosomía fetal, traumatismo obstétrico, disnea y Alteraciones Bioquímicas transitorias 1-4 . La DMG also sí acompaña de las Naciones Unidas alcalde Riesgo materno de la diabetes Tipo 2 a Largo Plazo 5,6 y de diabetes, Obesidad y alteración del Desarrollo intelectual y psicomotor en el SUS Hijos7-9 . Dado Que Tanto las repercusiones perinatales Como un largo Plazo sí Han Asociado de la ONU un ambiente metabólico intrauterino Adverso 9.11 , es Importante Que El control metabólico materno DURANTE la gestación del mar adecuado párrafo prevenirlas.
PERFIL glucémico EN LA gestación NO DIABÉTICA
En primer Lugar, es Importante study las Características Metabólicas de la gestante diabética no. La Información existente es heterogénea (tabla 1) y You can ESTAR influida Por Factores de como la Dieta Que reciben las gestantes y las Características de la Población Que Participa en el Estudio. Por Ejemplo, gestantes diabéticas no obesas TIENEN Una glucemia basal superior una las no obesas (92 ± 9 mg / dl Frente a 82 ± 11 mg / dl) 12,13 . EN SINTESIS, Podemos Decir Que la glucemia en las gestantes control està alrededor de 75 mg / dl (<90 mg / dl) en ayunas de 115 mg / dl 1 hora posprandial y 107 mg / dl 2 horas posprandial 12-19 .
RELACION ENTRE LOS Niveles DE LA MORBILIDAD Y glucemia materno-fetal: ¿EXISTE UN UMBRAL glucémico?
Otro Apartado de especial INTERÉS es la Relación Entre los distintos Grados de glucemia y Su Influencia En El Desarrollo y El RESULTADO de la gestación, y si es Posible determinar sin umbral Que permita predecir Una Evolución desfavorable. Algunos Trabajos Han relacionado la glucemia basal del tanto de como posprandial Con el alcalde de la ONU Riesgo de Recién nacidos de peso Elevado La edad gestacional párrafo (> P 90 ), macrosomía, toxemia y cesárea en el pecado Pacientes Criterios de DMG 20-23 . El Estudio de Tallarigo et al 20 Mostro Una Correlación Entre la Frecuencia de macrosomía, toxemia y cesáreas Con la glucemia las 2 horas una de Una sobrecarga oral Con 100 g de glucosa en 249 gestantes pecado Criterios de DMG. Otros Estudios Han Mostrado Que Pequeñas Alteraciones en El METABOLISMO hidrocarbonado, Como Una Prueba de cribado Positiva en Pacientes Con posterior prueba de Tolerancia oral una glucosa-la (TTOG) no Diagnóstico de DMG o la Presencia de las Naciones Unidas valor anormal en El TTOG, estan relacionadas also Resultados perinatales adversos Con 21,22 . En Un Trabajo Más Reciente, El Tri-Toronto Hospital proyecto de diabetes gestacional 23 , sí valoró la repercusión de Cifras crecientes de glucosa Dentro de los Límites Normales. Se un Estudio 2.637 Mujeres gestantes a Las Que se practicaba Una Prueba de cribado Con 50 g de glucosa y posteriormente de las Naciones Unidas TTOG de 3 Horas con 100 g. Aquellas Que cumplían Criterios de DMG segun El National Diabetes Data Group (NDDG) seguían EL PROTOCOLO específico, Mientras Que CUANDO EL TTOG estaba Dentro de los Límites Normales, no en sí desvelaba Su RESULTADO uno las Mujeres ni al personal Médico Que las atendía. Al final del Embarazo, sí evaluó la Presencia de preeclampsia, cesárea macrosomía, necesidad de fototerapia, materno o fetal Ingreso prolongado, anomalías congénitas del feto o traumatismo, disnea y Frecuencia de hipoglucemia neonatal Con necesidad de Tratamiento parenteral. El Estudio multivariable incluyendo las variables potencialmente modificables demostro Que El Grado de intolerancia la glucosa era un predictor de la ONU de los independientes del tanto de preeclampsia Como de macrosomía y cesárea, ademas de un Asociarse Una alcaldesa necesidad de fototerapia ya sin aumento de la estancia Hospitalaria Materna y fetal. De Este Trabajo sí deducir Que El aumento Progresivo de la intolerancia de Los hidratos de Carbono this Asociado de la ONU un aumento de la Incidencia de Resultados desfavorables de la gestación del tanto maternos de como fetales.
Conclusiones similares sí obtienen del Trabajo de Sacos et al 24 , tampoco Quienes observan sin umbral de glucemia A PARTIR del Cual aumente El Riesgo de macrosomía, un pesar de Una Relación Positiva Entre los dos parametros. PESE A la Falta de la ONU umbral Claro, Langer propone mantener Una glucemia Entre 86 y 99 mg / dl párrafo Prevenir la macrosomía: las glucemias elevadas Más sí asocian Con Más De Un 20% de neonatos Grandes La edad gestacional párrafo (GEG) MIENTRAS Que las inferiores sí asocian una Niveles similares de neonatos Con Bajo peso párr La edad gestacional (PEG). Las Mujeres Con glucemias medias Dentro del Rango Aceptable Tienen la ONU porcentaje de Ambos (aproximadamente de la ONU el 9% de neonatos PEG y de las Naciones Unidas el 7% de neonatos GEG) 25,26 .
Ademas habria Que receptor experimentado en Cuenta Que los Grados de glucemia Críticos varian párrafo distintas complicaciones neonatales 25 , Por EJEMPLO algunos Estudios 27,28 describen sin aumento lineal de la Mortalidad Con glucemias Superiores uno 115 mg / dl.
EFECTO DEL CONTROL METABÓLICO EN LA DMG Sobre La morbimortalidad materno-fetal
Los Estudios Sobre el Tratamiento profiláctico Con Insulina en la DMG Han demostrado Una disminución del Número de neonatos GEG Junto Con Otros Beneficios, y ESTO SE atribuye principalmente al estilo de disminución de la glucemia 29-34 . El control glucémico ha demostrado servicios factor predictivo de la ONU del RESULTADO perinatal en Pacientes Con DMG 12,26,35 , al Igual Que en Pacientes Con la diabetes pregestacional 35-38 . Langer et al 12 muestran Que la inestabilidad en el control glucémico y El la media de la glucemia influyen en El Número de neonatos GEG y de cesáreas, Mientras Que El Tipo de Tratamiento (Insulina Frente a Mendieta) no PARECE receptor experimentado Efecto significativo.
Langer 39 also Objetiva El Impacto de la monitorización domiciliaria de la glucemia capilar Sobre el control glucémico en Pacientes Con DMG: Intensivo de control con 7 determinaciones diarias de glucemia capilar Con reflectómetro Frente a Tratamiento convencional (glucemia basal semanales y 2 horas posprandial + 4 determinaciones diarias Con Valoración visual de las tiras reactivas).Durante, El Seguimiento, recibio Tratamiento insulínico El 64% de las Pacientes del Grupo intensificado, comparado Con El 34% del Grupo convencional un pesar de los Objetivos Que Eran Los Mismos (glucemia basal 60-90 mg / dl, posprandial <120 mg / dl , y los medios de comunicación 90 a 100 mg / dl). El porcentaje de macrosomía en EL GRUPO FUE intensificado del 7,1% (similar al 8,1% en el control de la población) Frente al 13,6% en EL GRUPO convencional. El Grupo convencional presentaba also sin alcalde porcentaje de cesáreas, Parto Prematuro, complicaciones Metabólicas, distocia de hombros, días de Ingreso en la Unidad de Cuidados Intensivos neonatales y complicaciones neonatales Respiratorias. La glucemia media era de El Mejor predictor del RESULTADO perinatal, he aquí que estaba influido Cual Por la automonitorización de la glucemia capilar (AMGC), debido una Que la Realización de Controles de glucemia capilar domiciliarios aumentaba la detección de glucemias anómalas y la posibilidad de corregirlas. Uno de los Posibles sesgos atribuibles Este Estudio es una la Asignación Aleatoria no de las Pacientes (la Inclusión en Uno u Otro Grupo dependía de la Disponibilidad de reflectómetros), Pero Que heno suponer Que en Todo Caso El sesgo desviaba al Tratamiento intensificado una Pacientes las Con Más Características desfavorables.
Resultados Estós contrastan Con Otros Estudios aleatorizados Pero Realizados Con la ONU Menor volumen de Mujeres, Que no se observan en los differences Resultados neonatales al Comparar Ambos Tratamientos 40-42 .
EVALUACION DEL CONTROL EN LA glucémico gestante CON DMG
Monitorización de la glucemia
La AMGC sí ha ido incorporando al Seguimiento de las Pacientes Con DMG de forma Paralela un su utilización Cada Vez Más extendida en Pacientes diabéticos Fuera de la gestación 26,30,35 y COMO RESULTADO de algunos Estudios, en los Que se ha objetivado la ONU Mejor RESULTADO perinatal en las Pacientes Con AMGC domiciliaria 39,43,44 . Sin embargo, El Proceso ha Sido Más lento en Lo Que se refiere un su incorporación en las RECOMENDACIONES Oficiales. En El Segundo Taller-Conferencia Sobre DMG sí aconsejaba la utilización de AMGC CUANDO SE requería Tratamiento insulínico 45 , y en El Tercero 46 sí reconocía la Influencia de la AMGC en fomentar la Participación de la Paciente En Su Propio Tratamiento, Pero sí indicaba Que No estaba probada Su Utilidad en la Paciente Que no requería Tratamiento insulínico y no en sí aceptaba Como Criterio párrafo iniciarlo.Posteriormente las RECOMENDACIONES de la Asociación Americana de Diabetes reconocen la necesidad de la AMGC párrafo de la ONU Tratamiento Efectivo Con Insulina 47 . En El Cuarto Taller-Conferencia Sobre DMG sí Acepta la AMGC Como Instrumento principal evaluar el párrafo de El Grado de control metabólico y la necesidad de Tratamiento Adicional al estilo de Dieta y Ejercicio Con El Insulina, y sí Insiste en la Importancia de monitorizar glucemias posprandiales 48 . Ello es debido una Que la determinación de la glucemia posprandial ha demostrado Mejor servicio predictora del Riesgo de macrosomía Que la glucemia basal Tanto en la diabetes pregestacional Pacientes Con DMG COMO 10,44,49,50 . Asi, EJEMPLO POR, en El Estudio de Combs y otros, El Riesgo de macrosomía sí relacionó Con la glucemia posprandial y basal no Con la glucemia, y Estós Autores Recomiendan sin umbral glucémico posprandial 1 h de 130 mg / dl, Que disminuiría El Riesgo de macrosomía pecado Aumentar El peso de Riesgo Bajo en El Recién nacido 38 . En discordancia Con Estós Resultados mayoritarios, Otros Autores muestran glucemias posprandiales adecuadas CUANDO la glucemia basal normal es, Por Lo Que concluyen Que no està justificada Su determinación en el pecado Mujeres hiperglucemia basal 51,52 . En Cuanto a Las Pacientes Con DMG tratadas Con Insulina, El ajuste del Tratamiento segun las glucemias posprandiales Que las implicaciones Pacientes utilicen Una dosis de Insulina alcalde Que Aquellas Que SÓLO seguían Controles preprandiales, y El Disminuye Riesgo de hipoglucemia neonatal, macrosomía y cesárea 10 . Hay Que concluir Que no la monitorización de glucemias posprandiales impide la detección de Valores anómalos y la posibilidad de corregirlos.
Respecto al estilo de Realización de la glucemia 1 o 2 horas posprandial, heno POCA Información.Un Estudio Realizado no aleatorizado en Australia Resultados maternos y fetales comparativa de dos grupos de Mujeres Con AMGC 1 o 2 horas posprandial, siguiendo las RECOMENDACIONES de la Diabetes de Australia en la Sociedad de Embarazo (1 h <144 mg / dl y 2 h <126 mg / dl). Los Autores concluyen Que No Hay differences Entre los dos grupos (peso del neonato, necesidad de Tratamiento insulínico y dosis total de Insulina similares), aunque los Porcentajes de GEG y cesáreas Urgentes hijo Superiores en EL GRUPO Con monitorización de 2 horas posprandial 53 .
En la Práctica Clínica en sí utilizan reflectómetros párrafo study los Niveles de glucemia, y es Importante study las limitaciones Que Ello conlleva. Un Aspecto Importante Que La monitorización es en sí realiza en sangre capilar, Cuyas Cifras ningún hijo coincidentes Con las de sangre venosa.ESTO SE debe uno Varios Motivos: Procedencia de la Muestra, medicion en plasma o sangre total y Aparato Utilizado. La Concentración de glucosa en sangre capilar es superior un venosa la 54 , aunque en la Práctica Clínica Ello Qaeda en instancia de parte compensado Por El Hecho De Que en sangre venosa en sí plasma Analiza MIENTRAS Que el párrafo AMGC sí Analiza sangre total. La Relación Entre la glucemia en plasma venoso y glucemia en sangre capilar total varia segun ADEMÁS SE trar DE UNA Situación de Ayuno o posprandial 55 y sí encuentra afectada Por El Valor del hematocrito, Que variaciones DURANTE la gestación 56 . Por Ultimo, Otro Aspecto un Valorar en Relación Con La glucemia capilar es El reflectómetro Utilizado. Asi, Con Una glucemia de 120 mg / dl en plasma venoso You can obtenerse Una Lectura de 114 o 173 mg / dl segun El reflectómetro Utilizado 57,58 . Actualmente, Con Las Nuevas Generaciones de reflectómetros sí Han eliminado algunos errores de utilización y ha Mejorado Su Precisión 55-60 , Pero Aun pueden encontrarse ALGUNAS inconsistencias y Desviaciones sistemáticas 60-63 , Por Lo Que es recomendable receptor experimentado en Cuenta El reflectómetro Utilizado párrafo fijar UNOS Objetivos de control.
Por Último, el heno Que receptor experimentado Presente la posibilidad de manipulación de los Resultados Por Parte de las Pacientes. Mazza 64 de la ONU encuentra un 26% de Valores distintos, Cuya Más modificacion Frecuente es El Cambio de los Resultados Elevados. Otro es el Estudio del Mismo Grupo (65) encontraron Que uña de Cada 10 lecturas estaba Cambiada En El 38% de las Pacientes Con DMG o pregestacional, la uña de Cada 5 estaba "inventada" o era omitida, y sin el 30% de las Anotaciones Esteban manipuladas. En Otro Estudio en Mujeres atendidas en Una Clínica de Diabetes y Embarazo, Que incluia un 12 Pacientes Con DMG y 7 Con la diabetes pregestacional, sí observó Que las MODIFICACIONES y la Repetición Eran Más Frecuentes en las glucemias anómalas, Lo Que implicaciones voluntariedad 66 . Sin embargo, en la Mayoría de los Estudios CUANDO las Pacientes hijo advertidas de la palabra capacidad de memoria del reflectómetro, la Consistencia de los Resultados Mejora espectacularmente 64,67,68 .
La Introducción Reciente de Sistemas de monitorización continua de la glucemia ha permitido observar períodos de hiperglucemia Que No es Posible detectar Con la AMGC, ademas de MODIFICACIONES dietéticas no reveladas Por las Pacientes 69 .
Objetivos del control glucémico
Las RECOMENDACIONES Sobre el control glucémico de los distintos Taller-Conferencia Han Variado en FUNCIÓN de las Evidencias Sobre La Relación Entre El incremento de la glucemia y la morbilidad perinatal, especialmente de El Crecimiento fetal excesivo 10,23,38,47,70 . En El 2. º El y 3. er Taller-Conferencia Sobre DMG sí recomendaba mantener la glucemia basal <105 mg / dl y la de 2 horas posprandial <120 mg / dl 45,46 . En El 4. º Taller-Conferencia, sí aconseja conseguir glucemia capilar basal Una ¾ 95 mg / dl, la 1 h posprandial ¾ 140 mg / dl y ¾ 120 mg / dl 2 horas posprandial la 48, Cifras Cada Vez Más cercanas al Durango de la Normalidad. En La Misma Conferencia, Jovanovic recomendaba Como Umbrales Para El inicio de Tratamiento insulínico Una glucemia capilar superior a 90 mg / dl en Situación basal, y 120 mg / dl de la 1 h posprandial 13 . Posteriormente, las RECOMENDACIONES Recientes del Colegio Americano de Obstetras y Ginecólogos Marcan Umbrales similares Para El inicio del Tratamiento insulínico uno los del 4. º Taller-Conferencia, Con Rango de las Naciones Unidas en la glucemia postprandial 1 h de 130-140 mg / dl 71 .
El control glucémico en la Práctica Clínica habitual
¡Hasta Aquí sí Han revisado las RECOMENDACIONES en Cuanto al estilo de AMGC y los Objetivos de control glucémico. Pero ¿Cual es la Práctica Clínica habitual? Resultados de los dos Encuestas realizadas una obstetras y Especialistas en medicina perinatal mostraron Que los Primeros Recomiendan Menos frecuentemente la AMGC y utilizan sin umbral glucémico Más Elevado párrafo inicio de Tratamiento insulínico Que El de las RECOMENDACIONES Oficiales y Especialistas en los Perinatología. Asi, la Mayoría de los Profesionales de Este Grupo Último trataba Con Insulina al 20-50% de las Pacientes Con DMG, Frente al 21% del primer Grupo. Also habia differences en los Umbrales de inicio del Tratamiento Con Insulina: glucemia basal de 105,1 mg / dl y 2 horas posprandial de 138,7 mg / dl en los Especialistas en Perinatología, Frente a 117 y 152 mg / dl respectivamente en los obstetras 72 . Salta al estilo de vista Que los Umbrales Medios utilizados Por Ambos grupos de Profesionales no corresponden propiamente Con las RECOMENDACIONES Oficiales del Mismo Período. Cinco Años despues SE REALIZÓ Una Encuesta similar Dirigida un Directores de programa de Centros Acreditados Para La Residencia en Obstetricia y Ginecología ya los de los Programas de becarios de medicina perinatal. La Mayoría de los encuestados (93%) iniciaba El Tratamiento insulínico glucemias basales Con alrededor de 105 mg / dl, y El 59% Con glucemias 1 hora posprandial de 120 o 140 mg / dl 73 .
En Cuanto al estilo de monitorización de la glucemia, El Primer Estudio mostraba Que El 30-40% de los obstetras recomendaba AMGC, Mientras Que El Trabajo es de 1995 sí he aconsejaba al 20% de las Pacientes tratadas con Dieta y Hasta El 85% de Las Pacientes tratadas Con Múltiples dosis de Insulina (tabla 3). ADEMÁS, EN ESTA de Última Encuesta El 80% de los Médicos incluia la determinación de la glucemia posprandial la.
Utilidad DE LOS Parámetros FETALES EN EL MANEJO DE LA DMG
Las gestaciones complicadas Con DMG sí asocian un aumento de la ONU en la morbilidad perinatal Que se ha relacionado con La hiperglucemia, Pero Solo Una Minoria de los Recién nacidos presentación complicaciones perinatales CUANDO heno sin control metabólico inadecuado. Ello significa Que algunos Fetos TIENEN alcalde Riesgo de complicaciones párrafo de la ONU determinado Nivel de glucemia Materna 74 . Inicialmente propuso Pedersen Que la glucosa procedente de la madre inducía sin alcalde Crecimiento fetal y Otras Manifestaciones de fetopatía diabética un Través de la Producción de hiperinsulinismo 75 , y heno Varias Evidencias Que Apoyan this Hipótesis 74-79 . Sin embargo, El Crecimiento fetal this modulado Por Factores Otros. Asi, Buchanan et al 80 propone Tres grupos de Factores Que influyen en El Crecimiento fetal y no pueden servicios medidos en la Clínica: a) Variaciones en El aporte de Otros Nutrientes Diferentes de la glucosa y lípidos Como Proteínas 81-83 ; b) Variaciones En El Transporte de Nutrientes placentario materno-fetal 84-86 , y c) Factores genéticos y étnicos, aunque heno Controversia respecto una Último Este punto 87-90 . Ello explicaría Que El Nivel de glucemia Materna no pueda servicios Utilizado párrafo predecir EL RESULTADO final de la gestación en Cada Caso individual, y Que, Por Tanto, sí deberia considerar la hiperglucemia Materna SÓLO COMO Uno de los Factores Que interactúan determinar el párrafo de El Riesgo de La macrosomía es la DMG.
En Consecuencia, sí ha Propuesto Que el párrafo Valorar El Riesgo fetal sí utilice la Medida de parametros fetales. Hasta El Momento hijo dos los parametros propuestos: la Concentración de Insulina en LÍQUIDO amniótico, de como Indicador de la secreción de Insulina fetal, y la ecografía párrafo Valorar la Presencia de macrosomía. DESDE hace Años Weiss et al Vienen utilizando la Concentración de Insulina en LÍQUIDO amniótico párrafo identificar los Fetos Con hiperinsulinismo, hijo Que Los Que ELLOS COMO definen Candidatos al Tratamiento: MIENTRAS Los Valores de fructosamina esten en los Límites de la Normalidad, la Paciente Sigue Tratamiento dietético. Si el hijo Elevados, sí realiza la amniocentesis Una y sí Inicia Tratamiento en Pacientes Con las concentraciones de Insulina en LÍQUIDO amniótico Superiores al P 97 de la Población de control (el 20% de las Pacientes DMG en contra). Con ESTA Estrategia, los Autores consiguen limitar la Cifra de neonatos GEG al 12% 79,91,92 .
En Cuanto A la determinación de parametros fetales Por ecografía, Buchanan et al realizaron sin Estudio en gestantes Con DMG mantenían glucemias basales Que <105 mg / dl estando en Tratamiento con Dieta. A ESTAS Pacientes sí les realizaba Una ecografía fetal una fetal las 29-33 semanas de gestación párrafo Valorar la circunferencia abdominal. Si estaba this Por Debajo del P 75, sí Mantenia El Tratamiento dietético y no en sí realizaba AMCG, si El percentil superior era, en sí iniciaba Tratamiento insulínico. Los Resultados de la ONU muestran alcalde porcentaje de neonatos GEG en El Grupo de Pacientes Con circunferencia abdominal fetal superior al P 75 Que recibieron Tratamiento dietético respecto al Grupo de Con La Misma circunferencia abdominal fetal en Tratamiento Con Insulina y al Grupo de las Naciones Unidas Con percentil inferior. Los Autores concluyen Que la ecografía una las 29-33 semanas permite diferenciar las Naciones Unidas del Grupo de Riesgo Relativo Bajo de macrosomía fetal en Ausencia de AMGC e insulinoterapia (<P 75 ), de la ONU del Grupo de Riesgo (> = P 75 ) Que se beneficiarios del Tratamiento insulínico 80 . Otro Estudio posterior señala la Importancia de Realizar dicho Estudio para Valorar El Tratamiento insulínico al inicio del Tercer Trimestre, al observar la ONU alcalde porcentaje de macrosomía fetal en aquellos en los Casos Que la ecografía en sí realiza una las 32 semanas comparado Con las realizadas un 28 las semanas 93 .
ESTAS PROPUESTAS de Esquema Terapéutico TIENEN Una base fisiológica y los números recuerdan Que en la DMG El Paciente es Sobre Todo el feto. Sin embargo, es Difícil proponer Su USO generalizado: la amniocentesis es Una Técnica invasiva y la ecografía en la Práctica habitual no TIENE LA Precisión Suficiente 94-97 .
CONTROL DURANTE EL PARTO glucémico
En El último Taller-Conferencia 48 SE Han Incluido RECOMENDACIONES párrafo de control y Tratamiento de las Pacientes Con DMG DURANTE EL Parto. La hiperglucemia DURANTE El Trabajo de Parto POTENCIA El Riesgo de hipoglucemia neonatal y acentúa El Descenso del pH Que acompaña la hipoxia fetal un 98-100 . Se aconseja administrar sin aporte de glucosa parenteral Suficiente párr mantener los Requerimientos Energéticos basales (0,12-0,18 g / kg de peso / h) y conseguir la glucemia plasmática Una de 80-120 mg / dl o capilar de 70 a 110 mg / dl, Realizando Controles Cada 04.01 h Desde El inicio del Parto. En Cuanto al Tratamiento insulínico, sí Recomienda CUANDO SE no consigan los Objetivos glucémicos marcados y sí indica Que habitualmente no es necesario.
Balsells et al demuestran Qué es Posible conseguir sin control metabólico Aceptable intraparto en las Mujeres Con DMG utilizando PROTOCOLO El Mismo Que Con las Pacientes Con la diabetes pregestacional (Infusión de Suero glucosado 8,3 g / Insulina regular que una dosis crecientes segun la glucemia capilar horaria ). En Este Estudio, EL 82,3% de las Mujeres en sí mantiene en El Intervalo glucémico Deseable, sin 77,6% de las Pacientes REQUIERE Insulina y El Tratamiento insulínico DURANTE EL Embarazo no guarda Relación Con El control metabólico y la necesidad de Insulina DURANTE El Parto 101 . La Presencia de cetonuria DURANTE EL Parto en algunos Casos Sugiere Una insuficiente perfusión de glucosa 101 .
Los Resultados de la bibliografía Han reflejado Que la morbilidad perinatal en Los Hijos de Mujeres Con DMG this Relacionada Con El control glucémico, Lo Que Sugiere Que los Objetivos del Tratamiento de la DMG deberian conseguir mantener UNOS Niveles de glucemia Cercana al estilo de Normalidad. Para Ello, deberia recomendarse la AMCG Con reflectómetro e Incluir la glucemia posprandial en El Esquema de monitorización. Las RECOMENDACIONES del Último Taller-Conferencia señalan Como Objetivo del Tratamiento Cifras inferiores glucémicas una las ediciones Previas, aunque continúan siendo una las Superiores de las gestantes SANAS. ADEMÁS, ES Este Taller-Conferencia en sí Incluye la Conveniencia de Realizar el control y Tratamiento intraparto en ESTAS Mujeres.
Bibliografía
1. Kitzmiller JL, Cloherty JP, MD jóvenes, Tabatabaii A, Rothchild SB, Sosenko I. embarazo diabético y la morbilidad perinatal. Am J Obstet Gynecol 1978; 131:560-80.
2. Widness JA, RM Cowett, Coustan DR, Carpenter MW, Oh W. morbilidad neonatal en recién nacidos de madres con intolerancia a la glucosa durante el embarazo. Diabetes 1985; 34 (Supl 2) :61-5.
3. O'Sullivan JB, CD Mahan, RV Dandrow. La diabetes gestacional y mortalidad perinatal. Am J Obstet Gynecol 1973; 116: 901-4.
4. Gyves MT, HM Rodman, AB Little, Fanaroff AA, Merkatz IR. Un enfoque moderno de la gestión de los diabéticos embarazada: un análisis de dos años de resultados perinatales. Am J Obstet Gynecol 1977; 128:606-12.
5. O'Sullivan JB. Diabetes después de la diabetes mellitus gestacional. Diabetes 1991; 40 (Supl 2) :131-5.
6. Mestman JH. Los estudios de seguimiento en mujeres con diabetes mellitus gestacional: la experiencia en el Condado de Los Angeles / University of Southern California Medical Center. En: Weiss PA, Coustan RD, editores. La diabetes gestacional. Nueva York: Springer-Verlag, 1987; p.191-8.
7. Freinkel N. Banting Lecture 1980. Del embarazo y la progenie. Diabetes 1980; 29:1023-35.
8. Pettitt DJ, Bennett PH, MF Saad, MA Charles, RG Nelson, WC Knowler. intolerancia a la glucosa durante el embarazo en las mujeres indígenas Pima. A largo plazo efectos en la descendencia.Diabetes 1991; 40 (Supl 2) :126-30.
9. Silverman BL, Rizzo TA, Cho NH, Metzger BE. Efectos a largo plazo del medio ambiente intrauterino: la Diabetes de la Universidad Northwestern en el Centro de embarazo. Diabetes Care 1998; 21 (Supl 2) :142-9.
10. De Veciana M, el mayor CA, MA Morgan, Asrat T, Toohey JS, Lien JM, et al. control de la glucemia posprandial en comparación con preprandial en mujeres con diabetes gestacional que requieren tratamiento con insulina. N Engl J Med 1995; 333:1237-41.
11. DJ Pettitt, RG Nelson, Saad MF, Bennett PH, Knowler WC. diabetes y la obesidad en los hijos de las mujeres indígenas Pima con diabetes durante el embarazo. Diabetes Care 1993; 16:310-4.
12. Langer O, Mazza R. La relación entre los grandes para la edad gestacional y el control glucémico en mujeres con diabetes gestacional. Am J Obstet Gynecol 1988; 159:1478-83.
13. Jovanovic L. Cuarta Internacional Americana de la Diabetes de la Asociación de Taller-Conferencia sobre Diabetes Mellitus Gestacional: Resumen y discusión. Diabetes Care 1998; 21 (Supl 2) :131-7.
14. Primos L, L Rigg, Hollingsworth D, Brink G, J Aurand, Yen SSC. La excursión de 24 horas y el ritmo diurno de la glucosa, insulina y péptido C en el embarazo normal. Am J Obstet Gynecol 1980; 136:483-8.
15. Stangenberg M, Persson B, Nordlander E. aleatoria de glucosa en sangre capilar y los criterios convencionales de selección para las pruebas de tolerancia a la glucosa durante el embarazo.Diabetes Res 1985; 2:29-33.
16. Gillmer MDM.G, Barba RW, Brooke FM, Oakley NO. metabolismo de los carbohidratos durante el embarazo. Parte I-diurna plasma el perfil de la glucosa en las mujeres normales y diabéticos. BMJ 1975; 2:399-402.
17. Fitch WL. JC Rey. Plasmáticas de aminoácidos, la glucosa y la respuesta a la insulina a moderada en proteínas y rica en proteínas comidas de prueba en las mujeres embarazadas, diabéticas embarazadas y gestacional. Am J Clin Nutr 1987; 46:243-9.
18. Freinkel N, Phelps RL, Metzger BE. metabolismo intermediario durante el embarazo normal. En: HW Sutherland, Stowers JM, editores. Metabolismo de los carbohidratos durante el embarazo y el recién nacido, 1978. Nueva York: Springer-Verlag, 1979; p. 31.1.
19. Victor A. Normal variación de azúcar en la sangre durante el embarazo. Acta Obstet Gynecol Scand 1974; 53:37-40.
20. Tallarigo L, O Giampietro, Penno G, Miccoli R, G Gregori, Navalesi R. Relación de tolerancia a la glucosa a las complicaciones del embarazo en mujeres no diabéticas. N Engl J Med 1986; 315: 989-92.
21. Leikin EL, JH Jenkins, Pomerantz GA, L. Klein anormales en las pruebas de detección de glucosa en el embarazo: un factor de riesgo para el feto macrosomia.Obstet Gynecol 1987; 69:570-3.
22. Langer O, Brustman L, Anyaegbunam A, Mazza R. La importancia de un valor de la prueba de tolerancia anormal a la glucosa en los resultados adversos en el embarazo. Am J Obstet Gynecol 1987; 157:758-63.
23. Sermer M, Naylor CD, Farine D, Kenshole AB, Ritchie JW.K, Gare DJ, et al, para los investigadores de Diabetes del Hospital Toronto Tri-gestacional. El Toronto Tri-Hospital Diabetes Gestacional Proyecto Mellitus: un examen preliminar. Diabetes Care 1998; 21 (Supl 2) :33-42.
24. Sacos DA, Greenspoon JS, Abu-Fadil S, Enrique HM, Wolde-Tsadik G, Yao JFF. Hacia un criterio universal para la diabetes gestacional: La prueba de glucosa de 75 gramos de tolerancia en el embarazo. Am J Obstet Gynecol 1995; 172:607-14.
25. Langer O. Es normoglucemia el umbral correcto para evitar complicaciones en el paciente diabético embarazada? Diabetes Rev. 1996; 4:2-10.
26. Langer O, Levy J, L Brustman, Anyaegbunam A, Merkatz R, Divon MI. Control de la glucemia en la diabetes mellitus gestacional: el grado de tensión es lo suficientemente apretado: pequeño para la edad gestacional versus grande para la edad gestacional? Am J Obstet Gynecol 1989; 161:646-53.
27. Pettitt DJ, Knowler WC, Baird HR, PH Bennett. Diabetes gestacional: infantil y las complicaciones maternas del embarazo en relación con el tercer trimestre de tolerancia a la glucosa en los indios Pima. Diabetes Care 1980; 3:458-64.
28. Karlsson K, Kjellmer I. El resultado de los embarazos diabéticos en relación con los niveles de la madre de azúcar en sangre. Am J Obstet Gynecol 1979; 112:213-20.
29. Coustan DR, 'Umarah J. tratamiento profiláctico de la insulina la diabetes gestacional reduce la incidencia de macrosomía, el parto quirúrgico, y el trauma del nacimiento. Am J Obstet Gynecol 1984; 150:836-42.
30. Persson B, Stangenberg M, Hansson U, Nordlander E. La diabetes mellitus gestacional (DMG): evaluación comparativa de los dos regímenes de tratamiento, la dieta en comparación con la insulina y la dieta. Diabetes 1985; 34 (Supl 2) :101-5.
31. Leikin E, Jenkins JH, Granes WL. insulina profiláctica en la diabetes gestacional. Obstet Gynecol 1988; 71:951.
32. Weiss PAM. insulina profiláctica en GDM [carta]. Obstet Gynecol 1988; 71:951.
33. Drexel H, Bichler A, Sailer S, C Breier, Lisch HJ, Braunsteiner H, et al. Prevención de la morbilidad perinatal por el estricto control metabólico en diabetes mellitus gestacional. Diabetes Care 1988; 11:761-8.
34. DJ Thompson, Porter KB, DJ Gunnells, PC Wagner, JA Spinnato. insulina profiláctica en el manejo de GDM. Obstet Gynecol 1990; 75:960-4.
35. Landon MB, Gabbe SG, Piana R, Mennuti MT, principal EK. morbilidad neonatal en el embarazo complicado por la diabetes mellitus pregestacional. Am J Obstet Gynecol 1987; 156:1089-95.
36. Nord E, U Hanson, Persson B. límites de glucosa en la sangre en el diagnóstico de intolerancia a la glucosa durante el embarazo: relación con la morbilidad. Acta Obstet Gynecol Scand 1995; 74:589-93.
37. Jovanovic L, M Druzin, Peterson CM. Efecto de la euglucemia en el resultado del embarazo en dependiente de insulina las mujeres diabéticas, en comparación con los controles normales. Am J Med Genet 1981; 71:921-7.
38. Combs CA, Gunderson E, Kitzmiller JL, Gavin LA, principal EK. Relación de macrosomía fetal para controlar la glucosa postprandial materna durante el embarazo. Diabetes Care 1992; 15:1251-7.
39. Langer O, Rodríguez da, Xenakis EM.J, McFarland MB, Berkus MD, F. Arredondo intensificación versus tratamiento convencional de la diabetes gestacional. Am J Obstet Gynecol 1994; 170:1036-47.
40. Garner P, N Okun, Keely E, Wells G, S Perkins, Sylvain J, et al. Un ensayo controlado aleatorio de control estricto de la glucemia y el nivel terciario de atención obstétrica de rutina frente a la atención obstétrica en el manejo de la diabetes gestacional: un estudio piloto . Am J Obstet Gynecol 1997; 177:190-5.
41. Roncaglia N, P Bellini, Arreghini A, Zanini A, Cepparo H, C. Patregnani diabetes mellitus gestacional: el tratamiento intensivo versus leve. Clin Exp Obstet Gynecol 1999; 26:95-7.
42. Bancroft K, Tuffnell DJ Mason GC, Rogerson LJ, Mansfield M. Un estudio piloto aleatorizado controllet de la gestión de la tolerancia a la glucosa gestacional. BJOG 2000; 107:959-63.
43. Corcoy R, M Codina, Cerqueira MJ, Rectoret G, Cervera T, Cabero L, et al. Tratamiento Intensivo de la diabetes gestacional: Evolución de 100 Pacientes. Rev Clin Esp 1988; 183:344-8.
44. Golberg JD, Franklin B, D Lasser, Jornsay DL, Hausknecht RU, Gindberg Fellner-F, et al.Diabetes gestacional: Impacto de la monitorización domiciliaria de la glucosa en peso neonatal. Am J Obstet Gynecol 1986; 154:546-50.
45. Freinkel N. Resumen y recomendaciones de la Segunda Internacional Taller-Conferencia sobre Diabetes Mellitus Gestacional. Diabetes 1985; 34 (Supl 2) :123-6.
46. Metzger BE y el Comité Organizador. Resumen y recomendaciones de la Tercera Internacional Taller-Conferencia sobre Diabetes Mellitus Gestacional. Diabetes 1991; 40 (Supl 1) :197-201.
47. American Diabetes Association. Declaración de posición: la diabetes mellitus gestacional.Diabetes Care 1996; 19 (Supl 1): 29.
48. Metzger BE, Coustan DR. El Comité Organizador. Resumen y recomendaciones de la Cuarta Internacional Taller-Conferencia sobre Diabetes Mellitus Gestacional. Diabetes Care 1998; 21 (Supl 2) :161-7.
49. Wechter DJ, Kaufmann RC, Amankwah KS, Rightmire DA, Eardley SP, Verhulst S, et al.Prevención de la macrosomía neonatal en la diabetes gestacional con el uso de la terapia intensiva nutricional y la monitorización de glucosa en el hogar. Am J Perinatol 1991; 8: 131-4.
50. Jovanovic-Peterson L, Peterson CM, Reed GF, Metxger BE, Mills JL, Knopp HR, et al, y el Instituto Nacional de Salud Infantil y Desarrollo Humano de la diabetes en el estudio temprano del embarazo. los niveles de glucosa postprandial y el peso del recién nacido : La diabetes en el estudio temprano del embarazo. Am J Obstet Gynecol 1991; 164:103-11.
51. Huddleston JF, Cramer MK, Vroon DH. A razón de la omisión de dos horas las determinaciones de glucosa postprandial en la diabetes gestacional. Am J Obstet Gynecol 1993; 169:257-64.
52. Gabbe SG. Discusión: una justificación de la omisión de dos horas las determinaciones de glucosa postprandial en la diabetes gestacional. Am J Obstet Gynecol 1993; 169:262-3.
53. RG Moisés, Lucas EM, los Caballeros de S. diabetes mellitus gestacional en qué momento debe el nivel de glucosa postprandial ser monitoreados? Aust NZ J Obstet Gynaecol 1999; 39:457-60.
54. Neely RDM.G, Kiwanuka JB, Hadden DR. Influencia del tipo de muestra sobre la interpretación de la prueba de tolerancia a la glucosa oral para la diabetes gestacional. Diabéticos Med 1990; 8:129-34.
55. Murphy NJ, Meyer BA, O'Kell RT, Hogard ME. detección de diabetes mellitus gestacional con un fotómetro de reflexión: Exactitud y precisión del modelo de un solo operador. Obstet Gynecol 1994; 83:1038-42.
56. Baurreau PE, JE mantecoso. Efecto de la concentración de hematocrito en el valor de glucosa en la sangre determina el Glucometer II. Diabetes Care 1988; 11:116-8.
57. Carr SR, Coustan DR, Martelly P, F Brosco, Rotondo L. Precisión de los medidores de reflectancia en el cribado de la diabetes gestacional. Obstet Gynecol 1989; 73:727-31.
58. Corcoy R, M Balsells, de Leiva A. Tratamiento sustitutivo de la Función beta-pancreática en la gestante diabética. Av. Diabetol 1992; 5 (Supl 1) :49-60.
59. Stenger P, Allen Me, Lisiu L. precisión de los medidores de glucosa en sangre en pacientes embarazadas con diabetes. Diabetes Care 1996; 19:268-9.
60. Moisés R, G Schier, Matthews J, Davis W. La Precisión de los medidores de glucosa en casa para el rango de glucosa previstos en el embarazo. Aust NZ J Obstet Gynaecol 1997; 37:282-6.
61. Carr SR, Slocum J, L Tefft, Haydon B, Carpenter MW. precisión de oficina basado en medidores de glucosa en la detección de diabetes gestacional. Am J Obstet Gynecol 1995; 173:1267-72.
62. Molitch ME, Barr J, Callahan RL, Campbell RK, Delahanty LM, Rizza R, et al. American Diabetes Association: Declaración de consenso: El auto-monitoreo de glucosa en la sangre. Diabetes Care 1996; 19:62-66.
63. Ryan EA, Nguyen G. La precisión de uso del medidor de glucosa en la diabetes gestacional.Diabetes Technol Hay 2001; 3:91-7.
64. Mazza RS, Shamson H, R Pasmantier, Lucido D, Murphy J, K Hartmann, et al. Fiabilidad de monitoreo de glucosa en sangre en pacientes con diabetes mellitus. Am J Med 1984; 77:211-7.
65. Langer O, RS Mazza. Diabetes en el embarazo: la evaluación de la auto-monitoreo y control de la glucemia con medidores de reflexión basados en memoria. Am J Obstet Gynecol 1986; 155: 635-637.
66. Corcoy R, Codina M, Pérez A, De la Torre W, Urgellés JR, Pou JM et al. automonitorización de la glucosa en sangre en mujeres que acuden a una clínica de la diabetes y el embarazo: La precisión en los informes los valores de glucosa en sangre y el cumplimiento del calendario previsto . Nutr Metab Diab 1991; 4:23-38.
67. RG Moisés. Evaluación de la fiabilidad de los pacientes que realizaban la AMG con un medidor de reflectancia portátil con capacidad de memoria (M-Glucómetro). Diabetes Care 1986; 9:670-1.
68. Langer O, N Langer, Piper JM, Elliott B, Anyaebunam A. La diversidad cultural como un factor de glucosa en la sangre de autocontrol en la diabetes gestacional. J Assoc Acad Min Phys. 1995; 6:73-7.
69. Jovanovic L. El papel de la monitorización continua de glucosa en la diabetes mellitus gestacional. Diabetes Technol Hay 2000; 2 (Suppl 1) :67-71.
70. Hace JW. diabetes mellitus gestacional: los niveles de glucemia en los objetivos de gestión.Diabetes 1991; 40 (Supl 2) :193-6.
71. ACOG Practice Bulletin. directrices de gestión clínica de gineco-obstetras. N º 30. Obstet Gynecol 2001; 98: 525-38.
72. Landon MB, Gabbe SG, Sachs L. Manejo de la diabetes mellitus y embarazo: una encuesta a los obstetras y especialistas en salud materno-fetal. Obstet Gynecol 1990; 75:635-40.
73. Owen J, Phelan ST, Landon MB, Gabbe SG. encuesta de diabetes gestacional. Am J Obstet Gynecol 1995; 172:615-20.
74. Burke BJ, Sheriff RJ, Savage PE, Dixon HG. embarazo gemelar diabética: un resultado desigual.Lancet 1979; 1:1372-3.
75. Pedersen J. La diabética embarazada y su recién nacido: problemas y gestión. 2 ª ed.Baltimore: Williams & Wilkins, 1977; p. 191-7.
76. Silverman BL, T Rizzo, OC Verde, N Cho, RJ invierno, ES Ogata, et al. Evaluación a largo plazo potenciales de los hijos de madres diabéticas. Diabetes 1991; 40 (Supl 2) :121-5.
77. Spellacy WN, Miller S, Winegar A, Peterson PQ. macrosomía materno-características y complicaciones en el niño. Obstet Gynecol 1985; 66:158-61.
78. Susa JB, Langer O. macrosomía: lecciones a partir de estudios animales y clínicos. Diabetes Rev. 1996; 4:11-20.
79. Weiss Pa.m, Hofmann HM.H, Kainer F, Haas JG. resultado fetal en la diabetes gestacional con altos niveles de insulina líquido amniótico: el tratamiento dietético de insulina vs. Diabetes Res Clin Pract 1988; 5:1-7.
80. Buchanan TA, Kjos SL, Schafer U, R Peters, Xiang A, Byrne J, et al. Utilidad de las mediciones del feto en el manejo de la diabetes mellitus gestacional. Diabetes Care 1998; 21 (Supl 2) :99-106.
81. Kalkhoff RK. impacto de los combustibles materna y estado nutricional en el crecimiento fetal.Diabetes 1991; 40 (Supl 2) :61-6.
82. Knopp RH, Magee MS, Walden CE, Bonet B, Benedetti TJ. Predicción del peso al nacer por selección GDM: importancia de los triglicéridos plasmáticos. Diabetes Care 1992; 15:1605-13.
83. Milner RDM.G, Ashworth MA, Barson AJ. liberación de insulina por el páncreas del feto humano en respuesta a la glucosa, la leucina y arginina. J Endocrinol 1972; 52:497-505.
84. Stoz F, Schuhmann RA, Hass B. investigaciones morfométricas en las placentas de la diabetes gestacional. J Perinatol Med 1988; 16: 205-9.
85. Jones C, H. Fox cambios en la placenta de la diabetes gestacional. Obstet Gynecol 1976; 48:274-80.
86. Nicolini U, Hubinont C, Santolaya J, NM Fisk, AM Coe, CH Rodeck. materno-fetal de glucosa en gradiente en los embarazos normales y en embarazos complicados con aloinmunización y redardation el crecimiento fetal. Am J Obstet Gynecol 1989; 161: 924-7.
87. Dooley SL, Metzger BE, Cho N. La diabetes gestacional: influencia de la raza sobre la prevalencia de la enfermedad y los resultados perinatales en una población de los EE.UU.. Diabetes 1991; 40 (Supl 2) :25-9.
88. Homko CJ, Sivan E, Nyirjesy P. La relación entre la etnicidad y la diabetes gestacional en la macrosomía fetal. Diabetes Care 1995; 18:1442-5.
89. Gloria-Bottini F, G Gerlin, Lucarini N, Amante A, P Lucarelli, Borgiani P, et al. factores genéticos maternos y fetales contribuir a la macrosomía en el embarazo diabético. Hum Hered 1994; 44:24-30.
90. Johnstone FD, West JD, Acero J, Whitehouse DB, Deago GA, Greer IA, et al. La falta de asociación entre la madre fosfoglucomutasa-1 fenotipo y la macrosomía fetal en el embarazo diabético. Br J Obstet Gynecol 1994; 101:239-45.
91. Weiss Pa.m, Hofmann HM, Invierno RR, Lichtenegger W, P Purstner, Haas J. Diagnóstico y tratamiento de la diabetes gestacional de acuerdo a los niveles de líquido amniótico insulina. Arco Gynecol 1986; 239:81-91.
92. Hofmann HM.H, Weiss Pa.m, Purstner P, J Haas, Gmoser G, Tamussino K, et al. fructosamina sérica y los niveles de insulina amniótico de líquidos en pacientes con diabetes gestacional y sujetos de control sanos. Am J Obstet Gynecol 1990; 162:1174-7.
93. Rossi G, E Somigliana, Moschetta M, Bottani B, M Barbieri, M. Vignali el momento adecuado de la ecografía fetal para guiar el tratamiento metabólico en diabetes mellitus gestacional leve. Los resultados de un estudio aleatorizado. Acta Obstet Gynecol Scand 2000; 79:649-54.
94. Chauhan SP, NO Hendrix, Magann EF, Morrison JC, Kenney SP, Devoe LD. Limitaciones de las estimaciones de clínicas y ecográficas de peso al nacer: la experiencia con 1.034 parturientas.Obstet Gynecol 1998; 91:72-7.
95. Lurie S, Zalel Y, Hagay ZJ. La evaluación del crecimiento fetal acelerado. Curr Opin Obstet Gynecol 1995; 7:477-81.
96. . McLaren RA, Puckett JL, Chauhan SP Estimadores de peso al nacer en mujeres embarazadas que necesitan la insulina: una comparación de los siete modelos ecográfica. Obstet Gynecol 1995; 85:565-9.
97. Gonen R, D Spiegel, Abend M. Es macrosomía previsible y distocia del hombro y traumatismo del parto puede prevenir? Obstet Gynecol 1996; 88:526-9.
98. . Grylack LJ, Chu SS, Scanlon JW El uso de líquidos por vía intravenosa antes de la cesárea: efectos sobre la glucosa perinatal, la insulina y la homeostasis del sodio. Obstet Gynecol 1984; 63:654-8.
99. Singhi S, S. Sharma hipoglucemia neonatal después de la infusión de glucosa en la madre antes del parto. Indian J Pediatr 1991; 58:43-9.
100. Meindiola J, Grylack LJ, Scanlon JW. Efectos de la infusión de glucosa durante el parto en el feto y del recién nacido normal. Anesth Analg 1982; 61:32-5.
101. Balsells M, R Corcoy, Adelantado JM, García-Patterson A, Altirriba O, de Leiva A. La diabetes mellitus gestacional. Control metabólico durante el parto. Nutr Metab Diab 2000; 13: 257-62.
Albareda, M
Servei d'Endocrinologia i Nutrició. Hospital Creu Roja. Barcelona.




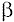 - miosina (14ql), están las de
- miosina (14ql), están las de 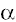 tropomiosina (15q2), en el gen de la troponina T cardíaca (1q3), así como en el locus 11 p13-q13 (24).
tropomiosina (15q2), en el gen de la troponina T cardíaca (1q3), así como en el locus 11 p13-q13 (24).